最新进展
PROGRESS
最新进展
PROGRESS
服务药企创新,助力高校科研-东大苏州医械院心脏芯片项目肩负重要使命
2021-11-19
心脏是人体循环系统的核心器官,包括了多层组织和不同类型的细胞:心肌细胞(心房肌和心室肌细胞)负责执行收缩功能、非心肌细胞(浦肯野细胞、平滑肌细胞、内皮细胞)及神经元细胞负责电信号的产生及传递。只有这些组织和细胞协同工作,精妙配合才可以确保心脏的正常运作,从而保障人体内正常的系统循环。由于心脏复杂的结构和发育机制使得在体外模拟心脏发育是一项困难的工作。尽管科学家们已经成功培育养出所有主要器官的类器官模型,但在心脏类器官领域的研发却始终进度缓慢,因此也限制了人类心脏病发生和预防等相关领域的研究。
近日,在《Cell》杂志上发表一篇题为“Cardioids reveal self -organizing principles of human cardiogenesis “的论文,该研究利用诱导人多能干细胞成功分化培养出体外自组织心脏类器官模型。该模型可通过经典wnt通路在体外模拟心脏发育,从而自发形成室样空腔形态,实现自主跳动。并借此来研究人类心脏疾病发生和其机制。

文章研究团队首先通过对关键信号通路分子的筛选,来模拟心脏的发育过程,并构建心脏类器官。这些关键分子包括:ACTIVIN、骨形态发生蛋白(BMP)、成纤维细胞生长因子(FGF)、维甲酸(RA)和WNT。同时,对人多能干细胞进行诱导分化以及3D高通量培养,发现心肌标志性基因ACTN2、TNNT2、TNNI1、MYL7、TTN、NPPA和ATP2A2均阳性表达。流式细胞仪检测显示心肌分化效率为90%,所形成的这些含空腔的组织称为心脏类器官。
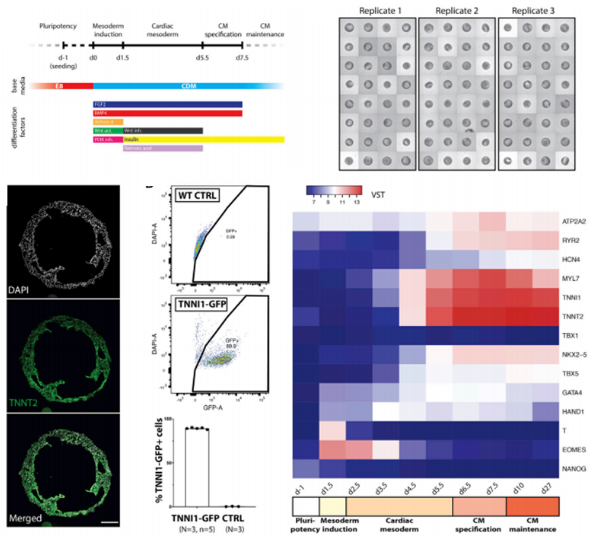
完成构建后,研究人员通过基因测序手段证实了体外心肌分化过程中表达人体中胚层关键标志。并论证了心脏类器官的空腔结构及心内膜的形成与Wnt和ACTIVIN通路密切相关,可通过对上述通路激动剂剂量调控心脏类器官发育过程中的内部结构。
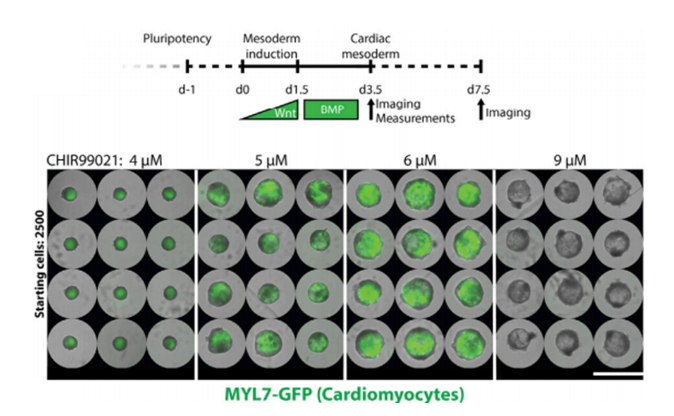
最后,研究团队通过冰冻损伤实验探究了心脏类器官的病理反应。结果显示,心脏类器官冰冻损伤模型可较好地模拟心脏受损后表现出的纤维化,证实了心脏类器官作为人类心脏疾病机制研究工具的潜力。
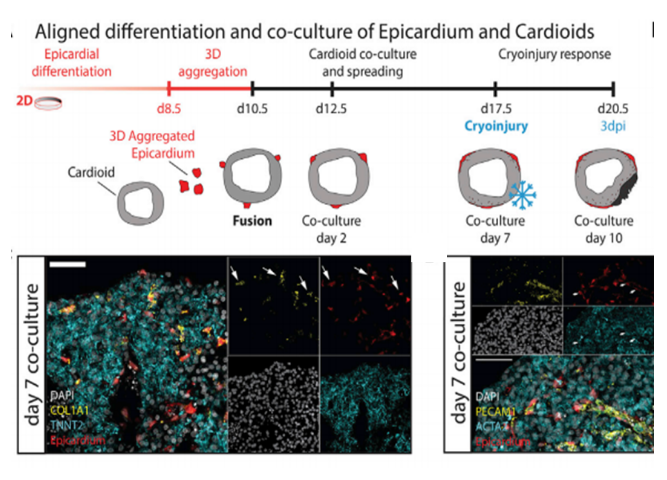
东南大学苏州医疗器械研究院紧跟国际一线研究,成功开发人体心脏芯片。我院自主构建的心脏类器官同样以人源性诱导多能干细胞进行自主分化组装并发育形成由心房肌、心室肌、窦房结及浦肯野细胞组成的多腔室可自发跳动的心脏类器官,通过微流控技术将心脏类器官集成培养在生物芯片上,从而构建出具有通量高、仿生高、成本低的人体心脏芯片,具有制备简单、稳定、可重复性好等优势,有较好的市场竞争力。人体心脏芯片可高度模拟人体心脏功能并实现心脏收缩、心肌钙瞬变、心脏信号传导及分子生化指标检测,适用于广大科研院所科学研究、药企心脏药物筛选和心脏毒性评价。
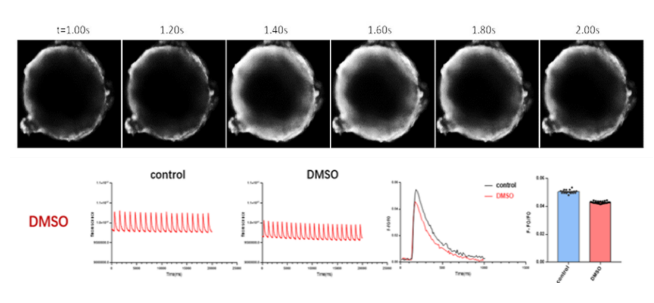
截止目前,东南大学苏州医疗器械研究院心脏芯片项目已成功与东南大学、华中科技大学、浙江大学等多家高校进行合作,同时为恒瑞、诺和诺德等国内外知名药企提供多轮技术服务并保持着心脏疾病模型构建合作,测试结果得到多家药企的高度认可。未来,东南大学苏州医疗器械研究院将会进一步推进心脏芯片项目的研发工作,积极开展人体心脏芯片在更多领域的探索及研究,持续与国内外药企合作提供技术测试服务,推动心脏领域药物的研发,为人类健康作出贡献。